戴建武团队成功在体外制造出含背/腹侧神经元的人脊髓组织
分子发育生物学国家重点实验室戴建武团队在脊髓组织体外制造研究中不断取得进展。团队在不久前建立了含有人神经干细胞和星形胶质细胞的脊髓组织制造技术,在体外实现了厘米级的临床可移植的脊髓组织制造(Jin et al Bioengineering & Translational Medicine,2022), 并通过材料与细胞共价偶联技术制造了具有药物靶向引导功能的人脊髓组织 (Liu et al, Science Advances, 2023)。
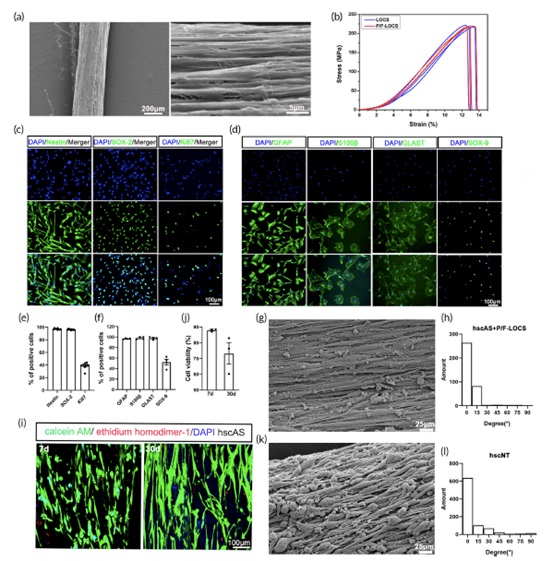
图1:厘米级的临床可移植的脊髓组织的制造
近期,团队在脊髓制造研究中又取得了新进展。研究人员通过诱导神经干细胞在胶原材料中预分化,制造出具有背腹侧结构的类脊髓组织(DV-SC),在移植到大鼠和恒河猴全横断脊髓损伤模型中后显示了良好的治疗效果。
研究人员利用神经分化信号因子组合对接种在胶原支架材料上的神经干细胞进行了为期30天的定向诱导分化,所获得的DV-SC中含有多种类型的脊髓背腹侧神经元,包括:BRN3A+ INs (背侧dilc-di3, diLB-di5神经元),TLX3+ INs (背侧di3, diLB-di5神经元),LMX1B+ INs (背侧diLB-di5神经元),LHX1+ INs (腹侧di6-V1神经元),FOXP2+ INs (腹侧V1神经元),HB9+以及ISL1+ (运动神经元)。

图2:体外制造具有脊髓背腹侧特征的人脊髓组织DV-SC
团队将DV-SC移植到大鼠和恒河猴T8-9完全性脊髓损伤模型中。DV-SC可以在大鼠和恒河猴损伤区更好地存活,产生成熟的功能性神经元。此外,DV-SC能够对应感觉和运动环路整合到宿主全横断的脊髓神经网络中,其中DV-SC来源的HB9+轴突和BRN3A+轴突可以分别和宿主5-羟色胺5-HT+轴突和降钙素基因相关肽CGRP+轴突形成靶向突触连接,部分恢复中断的神经回路,进而改善脊髓损伤大鼠和恒河猴的运动诱发电位和后肢运动功能的恢复。
该成果于3月30日在线发表在Bioactive Materials杂志上。该工作受到国家自然科学基金重大项目和中科院战略先导专项的资助。
附件下载: